| SOMMEILS ET INSOMNIES |
| Jean-Louis Valatx Pour la Science Janvier 1998 |
Pour s'endormir, il ne suffit pas d'éteindre la lumière. Les différents réseaux de neurones qui assurent l'éveil doivent être mis au repos par d'autres neurones. Des dysfonctionnements de ce système anti-éveil sont responsables d'insomnies.
Entre le mois d'avril et le mois de novembre 1918, la grippe espagnole a tué 25 millions de personnes dans le monde, dont plusieurs centaines de milliers de Francais. Certains malades avaient des lésions cérébrales (des encéphalites) qui se manifestaient soit par des insomnies, soit par une léthargie. A Vienne, le médecin Konstantin von Economo, observa chez des personnes décédées, que l'insomnie était associée à des lésions de l'hypothalamus antérieur et la léthargie à des lésions de l'hypothalamus postérieur. L'hypothalamus antérieur était-il le centre du sommeil et l'hypothalamus postérieur celui de l'éveil ?
Les observations cliniques de von Economo ont été confirmées sur des animaux ou l'on pratiquait des lésions par électrocoagulation. Puis, à la fin des années 1950, Michel Jouvet observa, chez l'animal endormi, une phase étonnante du sommeil, qu'il nomma le sommeil paradoxal, pendant laquelle surviennent les rêves. La localisation de l'activité onirique permit l'essor des recherches sur le sommeil. Enfin, la découverte des neurotransmetteurs du système nerveux central conjuguée à l'amélioration des techniques d'exploration du cerveau et à la miniaturisation des dispositifs d'enregistrement de l'activité des neurones ont aidé les neurobiologistes à élucider le fonctionnement des réseaux neuronaux du sommeil. N'oublions cependant pas que, malgré tout l'arsenal de techniques performantes dont on dispose, l'observation du comportement est la seule méthode de validation des résultats.
Les neurobiologistes ont récemment montre que l'éveil, indispensable à la survie, est garanti par tout un réseau de structures redondantes. Ils ont précisé les circuits neuronaux activés pendant l'éveil, ceux qui prennent le relais pour l'endormissement et le sommeil, et les perturbations qui engendrent des insomnies. Nous décrirons les structures qui maintiennent l'éveil, et comment la mise au repos de ces circuits déclenche le sommeil et le rêve, et enfin pourquoi Hypnos, le dieu du sommeil, refuse parfois de toucher les mortels de sa branche de pavot, leur refusant sommeil et rêves.
Qu'est-ce que le sommeil ?
Chez le chat, des enregistrements de l'activité électrique du cerveau ont permis l'analyse des différentes phases du sommeil. Après une période d'éveil ou cette activité électrique est rapide et de faible amplitude, l'animal présente les signes précurseurs du sommeil: il baille, cligne des paupières, fait sa toilette. Il cherche son lieu habituel pour dormir et prend la posture en sphinx, caractéristique de l'espèce féline, mais qui varie avec la température ambiante: le chat se met en boule quand il fait froid et s'allonge quand il fait chaud.
L'endormissement et le sommeil calme se caractérisent par la fermeture des paupières, l'immobilité et le ralentissement progressif des fonctions végétatives (la respiration, la fréquence cardiaque, la température et le tonus musculaire). Sur l'électroencephalogramme, on distingue deux stades de sommeil calme: le sommeil léger et le sommeil profond. Le sommeil calme dure entre 20 et 25 minutes (voir appendice).
Ensuite, le sommeil paradoxal associe des signes de sommeil profond, telle une absence de tonus musculaire, et des signes d'éveil, tels qu'un électroencephalogramme rapide, des mouvements oculaires et une respiration irrégulière. Le sommeil paradoxal a une durée moyenne de cinq a six minutes. Ainsi, un cycle de sommeil du chat dure environ une demi-heure. Après un bref éveil, un autre cycle commence.
Deux phénomènes caractérisent le sommeil paradoxal: les rêves et l'érection pénienne. On croyait ce dernier phénomène spécifique du sommeil paradoxal de l'homme, mais Markus Schmidt, dans notre laboratoire,l'a récemment mis en évidence chez le rat, réalisant ainsi le premier modèle experimental pour l'étude des mécanismes de l'érection au cours du sommeil paradoxal (il utilise un capteur miniature de la pression sanguine, dans le pénis). Il a ainsi montré que les neurones de l'érection au cours du sommeil sont situés dans une région de l'hypothalamus antérieur, proche (mais différente) de celle qui est responsable de l'érection durant l'éveil.
Seuls les vertébrés supérieurs, les oiseaux et les mammifères ont des cycles complets de sommeil, avec des phases de sommeil lent et des phases de sommeil paradoxal. Les durées de ces cycles varient d'une espèce à l'autre, et à l'intérieur même d'une espèce donnée. Chez l'homme adulte, la durée physiologique du sommeil dure de 3 à 12 heures. L'environnement physique (la température et la lumière) et social (l'isolement, le stress, les périodes d'apprentissage) agit sur la durée du sommeil.
Toutefois, ces facteurs n'expliquent pas toute la variabilité. En utilisant des lignées pures de souris, nous avons montré que certains facteurs, tels que la durée du sommeil, le nombre des mouvements oculaires pendant le sommeil paradoxal et la quantité de sommeil au cours de la récupération qui suit une privation de sommeil, sont héréditaires. Ces résultats ont été confirmés par l'étude de vrais jumeaux.
Les circuits de l'éveil
L'hypothalamus a longtemps été considéré comme le "centre de l'éveil". Puis, en 1949, Giuseppe Moruzzi et Horace Magoun déclenchent un coma, chez le chat, en lésant la formation réticulée. Ils supposent que ce coma correspond à une absence d'éveil. Comme la stimulation de la formation réticulée éveille l'animal endormi et que cette structure cérébrale recoit de nombreux messages véhiculés notamment par les voies sensorielles, ils proposent le concept de "système réticulé activateur ascendant" : la formation réticulée serait le centre de l'éveil. Le sommeil surviendrait lors de la mise au repos de la formation réticulée, après un certain temps de fonctionnement ou lorsque cessent les timulations éveillantes (la lumière, le bruit, etc.).
Puis l'utilisation des substances neurotoxiques qui détruisent seulement les neurones a infirmé les certitudes fondées sur des lésions obtenues par électrocoagulation. En 1992, Michel Denoyer et Marcelle Sallanon, dans notre laboratoire ont montré qu'une lésion de la formation réticulée et de l'hypothalamus postérieur ne perturbe pas durablement l'éveil. Ces résultats surprenants montrent que d'autres structures prennent le relais des structures détruites; les troubles de l'éveil qui avaient été obtenus antérieurement résultaient de la lésion des prolongements des neurones localisés dans les autres systèmes responsables de l'éveil. Ainsi, l'éveil est assuré par un réseau de structures redondantes.
De nombreux neuromédiateurs agissent dans ce réseau de l'éveil: des neurotransmetteurs "classiques" qui favorisent la transmission des messagers neuronaux, tels que l'acétylcholine, le glutamate, l'histamine, la noradrénaline et la sérotonine, d'autres médiateurs tels que des peptides (de petites protéines), des hormones, ou encore le monoxyde d'azote.
L'origine des neurones qui véhiculent ces neurotransmetteurs et les régions cérébrales qu'ils innervent ont été représentés sur la figure 2. Selon Kasuya Sakai, de notre laboratoire, les composantes de ce réseau se regroupent en deux systèmes : une voie centrale et une voie dorsale. Ces deux voies prennent naissance dans le bulbe rachidien. La voie ventrale se projette vers l'hypothalamus postérieur et le télencéphale basal (c'est la voie réticulo-hypothalamo-corticale). La voie dorsale active la formation réticulée mésencéphalique et le thalamus: c'est la voie réticulo-thalamo-corticale. Les différents neurotransmetteurs participent aux deux systèmes. L'acétylcholine et le glutamate y jouent un rôle important.
On a découvert assez récemment que l'histamine participe aussi aux mécanismes de l'éveil. Les neurones à histamine ont été localisés par Jian Sheng Lin, de notre laboratoire, dans l'hypothalamus postérieur. Ces neurones envoient des projections dans tout le cerveau antérieur, mais aussi dans le cerveau posterieur, sur les autres neurones de l'éveil. Par ailleurs, l'étude des substances pharmacologiques qui agissent sur l'histamine (inhibition de sa synthèse, action sur ses récepteurs) confirme que l'histamine participe à la régulation de l'éveil. Enfin, une observation clinique conforte ce rôle: les personnes à qui l'on administre des antihistaminiques contre les manifestations allergiques éprouvent souvent une certaine somnolence.
Les noyaux du raphé antérieur contiennent des neurones à sérotonine qui se projettent directement vers l'hypothalamus et vers le cortex. Longtemps, la sérotonine a été considérée comme l'hormone du sommeil, car la lésion des neurones qui la libèrent ou l'inhibition de sa synthèse provoque une insomnie de plusieurs jours. Toutefois, paradoxalement, ces neurones ne sont actifs que pendant l'éveil, et leur stimulation est éveillante.
En fait, on restaure le sommeil chez un animal rendu insomniaque par absence de sérotonine en lui injectant le precurseur immédiat du neuromédiateur dans l'aire préoptique de l'hypothalamus. Nous verrons que les neurones de cette région, sous l'influence de la sérotonine, participent au déclenchement du sommeil : il est donc logique que le manque de sérotonine dans l'hypothalamus empêche le sommeil. La sérotonine joue ainsi un double jeu spécifique: essentielle pour l'éveil, elle a un rôle fondamental dans le sommeil.
La noradrénaline vient surtout du locus coeruleus situé dans le pont de Varole (voir la figure 2). Ces neurones, actifs au cours de l'éveil, envoient des projections vers le cortex et vers le système limbique. Ils sont contrôlés par des neurotransmetteurs inhibiteurs, le GABA et la glycine, sur lesquels nous reviendrons. Recevant des signaux sensoriels et végétatifs, les neurones à noradrénaline jouent un rôle important dans les réactions au stress.
Figure 2 : Schémas des circuits de l'éveil
Schéma des circuits de l'éveil (1)
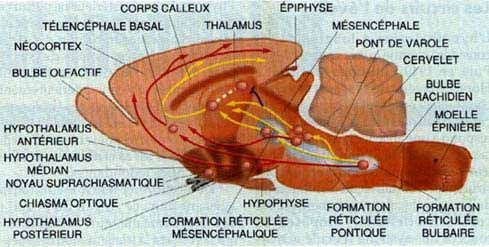
2. LES CIRCUITS DE L'EVEIL sont schématises (en haut a gauche) sur une coupe de cerveau de rat: la voie reticulo-thalamo-corticale dorsale (en jaune) et la voie reticulo-thalamo-corticale ventrale (en rouge). Différents neurotransmetteurs interviennent pour assurer l'éveil.
Schéma des circuits de l'éveil (2)
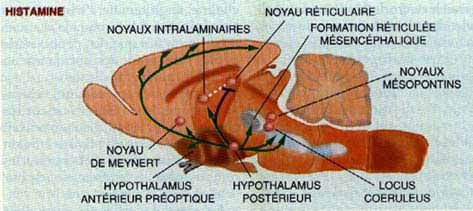
Les neurones qui libèrent l'histamine sont localisés dans l'hypothalamus postérieur. Ils se projettent sur l'ensemble du cerveau et notamment sur les autres neurones de l'éveil, et les activent (les flêches vertes).
Schéma des circuits de l'éveil (3)
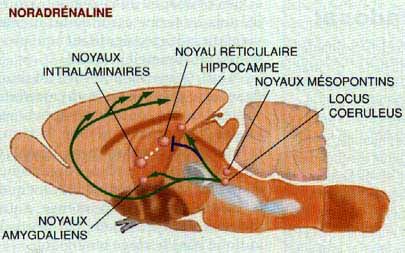
Les neurones qui produisent la noradrénaline sont localisés dans le locus coeruleus et émettent des prolongements vers le cortex, les noyaux amygdaliens et l'hippocampe.
Schéma des circuits de l'éveil (4)
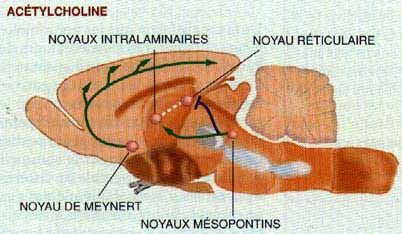
Les neurones à acétylcholine sont situés dans les noyaux mésopontins, qui se projettent notamment vers le thalamus, et dans le noyau de Meynert du télencephale basal.
Schéma des circuits de l'éveil (5)
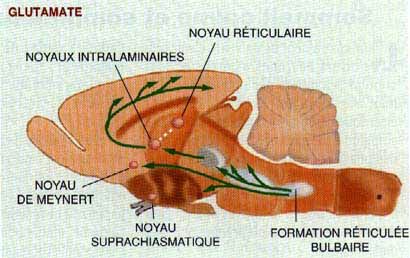
Les neurones à glutamate sont présents dans la formation réticulée bulbaire et mésencéphalique, et dans les noyaux intralaminaires du thalamus qui se projettent vers le cortex.
Schéma des circuits de l'éveil (6)
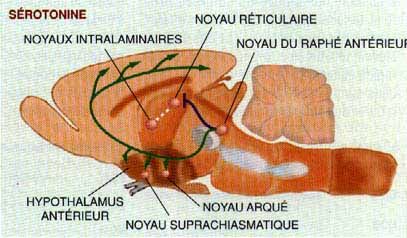
Les neurones à sérotonine sont situés dans le noyau du rapine anterieur et innervent le cortex et plusieurs noyaux de l'hypothalamus, tels l'aire préoptique, le noyau suprachiasmatique et le noyau arque. Le noyau suprachiasmatique est la principale structure de l'horloge biologique.
Les neurones à acétylcholine, à histamine, à noradrenaline, et à serotonine envoient des prolongements (les flêches bleues) vers le noyau réticulaire du thalamus pour l'inhiber au cours de l'éveil; lorsqu'ils cessent d'être inhibés, les neurones du noyau réticulaire déclenchent l'endormissement.
Les hormones et les peptides de l'éveil
Des peptides participent à la modulation de l'éveil. L'hormone CRH (Corticotropin releasing hormone) est synthetisée par de nombreux neurones, et elle active l'hypophyse et les glandes surrénales en cas de stress. Cette hormone a aussi une action cérébrale spécifique dans l'élaboration des réactions comportementales face aux situations nouvelles et au stress. L'hormone ACTH ou les endorphines (des substances antalgiques naturelles), libérées par les neurones de l'hypothalamus médian, stimulent le réseau de l'éveil (l'ACTH et les endorphines sont issues d'une même molécule, la pro-opio-mélanocortine).
On peut aussi inclure dans le système de l'éveil le noyau suprachiasmatique, la principale structure de l'horloge biologique. Une lésion du noyau suprachiasmatique abolit le rythme circadien des états de vigilance et de sommeil : les longues phases d'éveil diminuent, et leur répartition au cours d'une journée devient aléatoire.
Le noyau suprachiasmatique semble influer sur le rythme circadien par un de ses neuropeptides: la vasopressine. Les effets cérébraux de la vasopressine synthetisée par le noyau suprachiasmatique sont totalement différents de ceux de la vasopressine produite par l'hypophyse postérieure, qui agit notamment sur le rein et sur la pression arterielle.
Outre les neurotransmetteurs et les peptides de l'éveil qui activent le cortex, certaines substances sont éveillantes : par exemple, l'amphétamine ou le modafinil (Modiodal®). L'amphétamine agit en augmentant la durée d'action de l'adrénaline, de la noradrénaline et surtout de la dopamine dans les synapses.
Normalement, quand un neurotransmetteur est libéré par un neurone "amont", dit présynaptique, dans la fente synaptique (l'espace qui sépare le neurone amont du neurone "aval", dit postsynaptique), il active le neurone postsynaptique. Quand il a fini d'agir, il est recapturé par le neurone présynaptique par l'intermédiaire d'un "transporteur". L'amphétamine bloque le transporteur de la dopamine, de sorte que le neuromédiateur excitateur reste longtemps dans la fente synaptique et continue à agir, tant qu'il n'est pas dégrade par des enzymes. Bruno Giros et ses collegues de l'unite INSERM U288 ont montré que, chez des souris transgéniques qui ne synthétisent plus le transporteur de la dopamine, l'amphétamine n'agit plus, puisque sa cible principale a été éliminée. Apres un éveil prolongé dû à l'amphétamine, la durée du sommeil augmente, ce que l'on nomme l'effet rebond.
Le modafinil, une nouvelle molécule éveillante, procure un éveil calme sans effets secondaires ni rebond de sommeil. J.S. Lin a montré que le modafinil semble agir sur des récepteurs adrénergiques localisés dans une région précise de l'hypothalamus antérieur, tandis que l'amphétamine agit dans d'autres régions (notamment dans le cortex et dans le système limbique).
Ainsi, dans tous les cas énumérés, l'activation du cortex résulte de la stimulation directe des neurones corticaux par les différents éléments du réseau de l'éveil. Pour réaliser cette activation, envisageons une dernière possibilité: l'inhibition d'un système inhibiteur. Si l'on muselle un système d'inhibition, on renforce l'activation. Il existe essentiellement deux neurotransmetteurs inhibiteurs: le GABA et la glycine. Or, des neurones GABAergiques, localisés dans l'hypothalamus postérieur et dans le télencéphale basal, inhibent d'autres neurones GABAergiques corticaux. Ainsi, le rôle éveillant de l'hypothalamus postérieur s'exerce de deux façons: une stimulation directe par l'histamine et une stimulation indirecte par le GABA.
La régulation de l'éveil, vitale pour la survie, met en jeu plusieurs structures redondantes: aucune des structures décrites, prise isolement, n'est indispensable à l'activation corticale.
L'endormissement
Le réseau d'éveil, une fois activé, est entretenu par les stimulations internes et externes. Comment l'envie de dormir est-elle à nouveau déclenchée ? L'arrêt des stimulations ne semble pas suffisant. La sérotonine, qui joue un rôle notable dans l'éveil, participe aussi au sommeil. Nous avons vu que l'inhibition de la sérotonine entraîne une insomnie qui est levée par l'injection de son précurseur uniquement dans l'aire préoptique de l'hypothalamus. La lésion de cette région déclenche une insomnie de très longue durée (plus de trois semaines): ces deux résultats confirment le rôle hypnogène de la sérotonine.
Toutefois, l'insomnie due à une lésion de l'aire préoptique est interrompue par l'injection d'un analogue du GABA (le muscimol) dans l'hypothalamus postérieur, ou convergent plusieurs éléments du système d'éveil. Puisque l'insomnie cesse, nous pensons que l'aire préoptique n'est pas un "centre" du sommeil, mais plutôt une région qui contrôle l'éveil. Ainsi, une des composantes de l'éveil, la sérotonine, stimule, par certaines de ses terminaisons, l'aire préoptique qui, en retour, vraisemblablement par des neurones GABAergiques, inhibe l'ensemble du réseau de l'éveil : c'est un système ami-éveil qui facilite l'endormissement.
Le noyau du faisceau solitaire, dans le bulbe rachidien, intervient aussi dans l'endormissement par ses projections sur l'aire préoptique. Ainsi, dans les années 1970, Paul Dell et Jean Jacques Puizillout, à l'Universite de Marseille, ont montré que la stimulation de nerfs pneumogastriques endort un animal insomniaque. De plus, les pratiquants de sports de combat et les masseurs de Bali connaissent bien les effets sur la vigilance des atemis (des coups portes à la hauteur du cou) et des massages de la région carotidienne. Le terme carotide lui-même vient du mot grec signifiant "qui provoque un sommeil profond".
Ainsi, le système ami-éveil est situé dans l'aire préoptique, à un carrefour stratégique qui contrôle des fonctions vitales: la thermorégulation, la faim, la reproduction notamment. Il analyserait l'état fonctionnel de l'organisme et déclencherait le sommeil avant que la fatigue ne soit trop intense, à un moment du nycthémère (24 heures) indiqué par l'horloge biologique.
Le sommeil lent
De la même façon que les neurobiologistes ont décrypté les médiateurs de l'éveil, ils ont décodé ceux du sommeil. Le sommeil lent est défini négativement par les Anglo-saxons comme le sommeil qui n'est pas du sommeil paradoxal. Les neurophysiologistes ne disposent pas, comme pour le sommeil paradoxal, d'un ensemble de critères mesurables. L'immobilité n'étant pas un critère suffisant, c'est l'étude de l'activité électrique du cerveau qui a fourni les caractéristiques du sommeil lent : la présence de fuseaux et d'ondes lentes (voir apppendice). Mircea Steriade et ses collègues de l'Universite Laval, à Montréal, ont montré que cette activité électrique prend naissance dans le noyau réticulaire thalamique. Les neurones GABAergiques de ce noyau émettent des potentiels d'action périodiques qui entraînent une hyperpolarisation cyclique des neurones thalamiques se projetant sur le cortex. Ces hyperpolarisations sont à l'origine du blocage des messages sensoriels au début de l'endormissement (un neurone hyperpolarisé n'émet plus de messages). Le noyau réticulaire du thalamus est sous le contrôle inhibiteur des réseaux de l'éveil (l'acétylcholine, l'histamine, la noradrénaline).
Puis s'installe le sommeil profond. Les ondes lentes qui le caractérisent résultent de l'hyperpolarisation des cellules pyramidales du néocortex déclenchée par des interneurones GABAergiques locaux, vraisemblablement sous l'influence des neurones préoptiques. Le néocortex (une région du cortex apparue chez les mammifères) est nécessaire à l'apparition des ondes lentes: son ablation les supprime, mais l'animal sans neocortex a toujours un comportement de sommeil (difficile à quantifier en l'absence d'ondes lentes). Chez les vertébrés inférieurs (les reptiles, les amphibiens, les poissons), on n'enregistre pas d'ondes lentes de grande amplitude, car le néocortex n'est pas développé. Chez ces animaux, l'observation du sommeil lent est difficile.
Le sommeil paradoxal
En 1959, Michel Jouvet observait pour la première fois le sommeil paradoxal. Ses observations sur un animal décérébré lui ont d'emblée permis de localiser les structures responsables de ce type de sommeil dans le tronc cérébral. Les neurones SP-ON, spécifiquement activés durant le sommeil paradoxal y sont localisés: ils forment le système dit éxécutif du sommeil paradoxal.
Des groupes de neurones SP-ON ont été identifiés pour chaque composante du sommeil paradoxal. Ainsi, l'atonie musculaire résulte de l'hyperpolarisation des neurones moteurs de la moelle épinière par la glycine, un neurotransmetteur inhibiteur libéré par des neurones du tronc cérébral. Patrice Fort, dans notre laboratoire, a observé que les noyaux moteurs des nerfs crâniens sont peu soumis à l'action inhibitrice de la glycine, ce qui expliquerait la persistance des mouvements des yeux et de la face, au cours du sommeil paradoxal. Des neurones GABAergiques participent aussi à l'atonie musculaire.
Lorsque les neurones SP-ON sont activés, au début du sommeil paradoxal, les neurones SP-OFF s'éteignent. Les neurones SP-OFF forment le réseau dit permissif: pendant l'éveil, ils empêchent les neurones SP-ON du système éxecutif de fonctionner, et c'est parce qu'ils s'arrêtent que le sommeil paradoxal peut s'installer. Ce sont des neurones aminergiques (à noradrénaline, à sérotonine ou à histamine). Certaines hypersomnies résulteraient de l'arrêt prolongé du système permissif.
Chez le cobaye, au cours de la deuxième moitié de la gestation, le foetus est en état de sommeil paradoxal pendant 90 pour cent du temps. On sait que la myelinisation des neurones indique leur maturation (la myeline est la gaine qui protège les neurones et facilite la propagation de l'influx nerveux); elle commence dans le tronc cérébral (ou sont localisés les neurones du sommeil paradoxal). Pendant cette période, le réseau du sommeil paradoxal serait le seul à fonctionner en permanence. Progressivement, les neurones du systeme permissif deviennent fonctionnels et la durée du sommeil paradoxal diminue.
Chez l'adulte, on peut provoquer, pendant quelques heures une hypersomnie de type foetal par injection en des endroits très précis du tronc cérébral, de substances qui agissent sur des récepteurs du GABA, de l'acétylcholine ou du glutamate. La privation de sommeil est suivie d'une hypersomnie plus ou moins durable.
Cet effet rebond a été attribué à l'accumulation de substances hypnogènes produites pendant l'éveil prolongé. Toutefois, nous avons montré qu'en lésant les cellules qui produisent certaines substances hypnogènes, cet effet rebond est supprimé sans que le sommeil spontané ne soit modifié. Puisque l'effet rebond n'est pas nécessairement associé a un éveil prolongé, c'est que le rebond est produit par un mécanisme indépendant de celui du sommeil. En réalite, la suppression des substances hypnogènes a peu d'effet sur le sommeil. Ces substances ne sont pas hypnogènes au sens strict du terme, mais elles facilitent le sommeil en agissant sur divers composants du système permissif. On devrait plutôt les qualifier d'hypnagogues, c'est-à-dire qui conduisent au sommeil.
Raymond Cespuglio, dans notre laboratoire, a étudié l'effet d'un stress aigu ou chronique sur le sommeil paradoxal. Il a montré qu'en déclenchant un stress chez un rat (en l'immobilisant pendant une heure environ), au début de la nuit, ou il est normalement éveillé, on déclenche une augmentation de la durée du sommeil paradoxal pendant quelques heures. Le stress déclenche une libération de sérotonine dans le noyau arqué de l'hypothalamus et une synthèse accrue de substances hypnagogues. De plus, nous avons montré que la lésion neurotoxique des terminaisons noradrénergiques du locus coeruleus supprime l'hypersomnie qui survient après un stress de courte durée. Au contraire, le stress chronique (dont la durée est supérieure à quatre heures) entraîne une réduction du temps de sommeil, à cause d'une production excessive d'hormones surrénaliennes, notamment de cortisone. Chez l'homme, le traitement de certaines maladies par de fortes doses de cortisone réduit notablement la durée de sommeil.
En bref, l'augmentation de la durée du sommeil paradoxal, après un stress de courte durée, résulte de l'activation en cascade de plusieurs boucles de régulation qui renforce le système antiéveil. Les hypersomnies observées à la suite de séances d'apprentissage complexes résultent vraisemblablement de tels mécanismes.
Il nous reste à évoquer le rôle d'une hormone dans le sommeil paradoxal : celui de la prolactine, une hormone de la lactation, mais qui est aussi présente chez les mâles. Parmi ses nombreuses fonctions, elle participerait au contrôle du sommeil paradoxal. Ainsi, chez une lignée de rats ayant un déficit en prolactine, nous avons observé une anomalie du rythme circadien du sommeil paradoxal sans modification des durées du sommeil. Or, chez le rat sain, l'ablation de l'hypophyse, ou est produite la prolactine, n'entraîne pas cette anomalie du sommeil. Avec Luce Paut, nous avons mis en évidence un système neuronal indépendant de l'hypophyse et synthétisant la prolactine. Nous ignorons encore le mécanisme d'action de la prolactine, mais nous espérons l'élucider en étudiant le rôle des récepteurs de la prolactine découverts sur les neurones du réseau de l'horloge biologique.
En résumé, la régulation du cycle veille-sommeil-rêve comprend cinq éléments: les système de l'éveil, du sommeil lent et du sommeil paradoxal, le réseau de l'endormissement et l'horloge biologique qui assure le rythme circadien.
L'alternance du sommeil lent et du sommeil paradoxal semble avoir une origine métabolique. Au cours du sommeil paradoxal, le cerveau consomme autant de glucose et d'oxygène que pendant l'éveil. La durée du rêve dépend des réserves énergétiques disponibles. Au contraire, le sommeil lent économise l'énergie: le métabolisme général et la température corporelle diminuent, et les réserves énergétiques se reconstituent.
Le sommeil lent et le sommeil paradoxal étant commandés par des systèmes différents, on leur attribue des fonctions différentes. Ainsi, un exercice physique intense et une température ambiante élevée pendant l'éveil entraînent une augmentation du sommeil lent. Au contraire, la durée du sommeil paradoxal augmente à la suite de situations nouvelles mettant en jeu la survie (par exemple, un stress d'immobilisation ou une épreuve de labyrinthe). Au cours du sommeil paradoxal, les comportements caractéristiques de l'espèce s'expriment (voir appendice). Lorsque l'apprentissage est maitrisé ou lorsque l'animal est habitué au stress répété, le sommeil redevient normal. La privation de sommeil perturbe l'acquisition de la maîtrise de ces situations. Chez l'homme, la suppression prolongée du sommeil paradoxal ne semble pas perturber la mémorisation. Toutefois, les tests servant à l'évaluation des troubles de la mémoire ne mettent pas les personnes qui participent aux tests dans des conditions de survie aussi difficiles que les animaux.
Schéma du sommeil paradoxal
Schéma du sommeil paradoxal
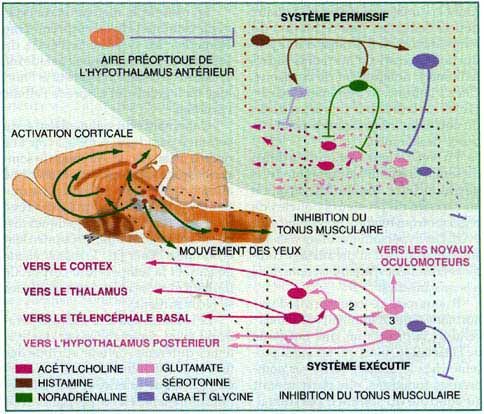
3. LE SOMMEIL PARADOXAL: les différents composants du réseau executif du sommeil paradoxal (le rectang/e noir en pointillés) ont été schématisés sur la coupe de cerveau de rat. Les neurones à acetylcholine (1 sur l'agrandissement, en bas à droite) stimulent notamment le thalamus et le télencephale basal; ils sont responsables de l'activité corticale rapide. Des neurones à glutamate (2) se projettent sur les neurones à acetylcholine, sur les neurones à GABA de l'hypothalamus postérieur, sur les noyaux oculomoteurs (les yeux bougent durant le sommeil paradoxal) et sur la formation réticulée bulbaire (3) responsable de la paralysie musculaire. Le reseau permissif (le rectangle rouge en pointilles, en haut a droite), empêche le déclenchement du sommeil paradoxal pendant l'éveil; il est constitué de neurones à sérotonine, à noradrénaline et à GABA, actifs pendant l'éveil et qui inhibent le réseau exécutif (les circuits non fonctionnels pendant l'éveil ont été schématisés par des traits en pointillés). Pour que le sommeil paradoxal s'installe, il faut que le système permissif soit lui-même inhibé: ce dernier est sous le contrôle du système anti-éveil de l'hypothalamus antérieur et d'autres neurones du tronc cérébral que l'on n'a pas représentés.
|
Une publicité pour un somnifère : "Ne soyez plus le seul éveillé quand toute la ville dort, prenez..." |
Les troubles du sommeil
Quelles sont les origines des insomnies ? Les troubles dus à des anomalies des réseaux du sommeil lent et du sommeil paradoxal semblent assez rares. Ils surviennent au cours des
maladies dégénératives ou traumatiques du système nerveux central. Les difficultés d'endormissement, qui ne sont pas dues à une maladie somatique ou psychiatrique, ne résultent généralement pas d'un trouble du sommeil, mais d'un trouble de l'éveil.
Deux hypothèses sont envisageables: la persistance de l'activité du réseau de l'éveil et l'hypoactivité du système anti-éveil. Divers facteurs du milieu exterieur - tels la lumière, le bruit, ou la température -, du milieu interieur - telles la faim, la soif, la douleur - et les stimulations affectives (les émotions ou l'anxiété) ou cognitives sont de puissants facteurs éveillants. Pour la sécurité, l'éveil est prioritaire: on doit se sentir en sécurité pour s'endormir.
Quand les facteurs précédents ne sont pas en cause, l'insomnie peut résulter d'une perturbation du réseau antiéveil, notamment d'une diminution de l'activité des neurones à sérotonine. Cela expliquerait l'effet somnifère de certains antidépresseurs qui augmentent la concentration de sérotonine dans la fente synaptique par inhibition de la recapture. L'hypoactivité résulterait de la dégénérescence neuronale due au vieillissement ou à un traumatisme.
Il existe d'autres types d'insomnies : l' hypnagnosie de Jouvet, c'est-à-dire la perception érronée du sommeil. Elle s'observe chez les personnes agées ou ayant subi une intervention chirurgicale avec une anesthésie prolongée. Ces personnes ne se souviennent pas d'avoir dormi, bien que les enregistrements montrent le contraire. Cette plainte résulte d'un trouble de la mémoire. La réeducation mnésique peut les aider à se souvenir de leur sommeil.
Certaines personnes ne s'endorment que très tard, et ce retard de phase de l'horloge biologique est souvent interprété comme une insomnie. Il réduit, effectivement, le temps de sommeil (quand la personne doit se lever pour aller travailler), ce qui entraîne une somnolence diurne excessive, avec son cortège d'effets indésirables: une inattention, une baisse de l'efficacité physique et intellectuelle, voire des accidents.
Quelles conséquences cliniques tire-t-on de ces constatations ? L'approche thérapeutique proposée est souvent comportementale: plus de la moitié des insomnies sont améliorées, sinon guéries, quand le médecin explique simplement aux patients comment se déroule une nuit de sommeil et quand il prodigue quelques conseils d'hygiène de vie (avoir une alimentation équilibrée, pratiquer un exercice physique modéré et régulier, mais pas le soir, ne pas boire de boissons excitantes en fin d'après-midi, se lever tous les jours à heure fixe, etc.).
En cas d'échec, le médecin aidera le patient à rechercher les causes de la stimulation excessive du système de l'éveil, et prescrira éventuellement des médicaments stimulant le système antiéveil: pour réhabituer les insomniaques à dormir, la prescription de somnifères pendant quelques jours est parfois nécessaire. La majorité des somnifères agit en se fixant sur des récepteurs GABA, c'est-à-dire en activant un circuit inhibiteur: le réseau de l'éveil est inhibé, mais ces somnifères ont l'inconveénient de perturber d'autres circuits, comme celui de la mémoire et de l'humeur. De surcroit, de nombreux somnifères entraînent une dépendance dont les personnes traitées doivent être averties. L'arrêt du médicament doit être progressif pour éviter le syndrome de sevrage (anxiété, cauchemars, insomnie). Une meilleure connaissance de la constitution du récepteur GABA permettra aux pharmacologues de mettre au point des molécules qui agiront plus spécifiquement sur le système anti-éveil.
Schéma de l'insomnie
Schéma de l'insomnie
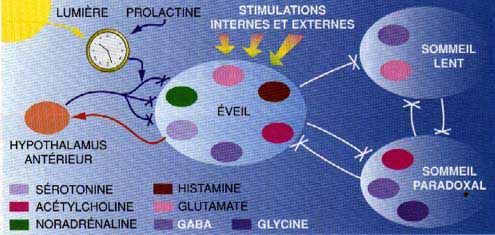
4. LES INSOMNIES résultent d'une inhibition insuffisante de l'éveil. Le système de l'éveil est assuré par plusieurs neurotransmetteurs excitateurs activés par les stimulus externes ou internes. Le système de l'éveil empêche le sommeil de se déclencher (les inhibitions sont schématisées ci-dessus par les croix). Quand ce système est mis au repos par le système ami-éveil localisé dans l'hypothalamus, les inhibitions exercées sur les neurones du sommeil lent et du sommeil paradoxal sont levées. C'est le système de l'éveil lui-même qui active le système anti-éveil, par l'intermédiaire d'une de ses composantes: la sérotonine.
Les hypersomnies
La narcolepsie est caracterisée par des accès invincibles de sommeil durant la journée, parfois accompagnés de paralysie musculaire (catalepsie), à l'origine d'accidents de la route ou du travail. Les émotions ou les horaires irréguliers de sommeil favorisent les crises chez les personnes génétiquement prédisposées. La narcolepsie est vraisemblablement un trouble du contrôle du système permissif du sommeil paradoxal. Des traitements pharmacologiques (notamment le modafinil) normalisent les accès narcoleptiques.
Les hypersomnies (lorsque la durée du sommeil dépasse 12 heures) résultent parfois d'une hypoactivité du réseau de l'éveil, ou d'un hyperfonctionnement du système ami-éveil. Seule une approche pharmacologique est aujourd'hui envisageable: de nombreuses molécules stimulent les composantes du réseau de l'éveil, mais on ne dispose pas encore de substances qui réduisent spécifiquement l'activité du système ami-éveil. Ces hypersomnies diffèrent de la somnolence diurne excessive, due au manque de sommeil ou à la perturbation du déroulement du sommeil nocturne par des troubles associés au sommeil, tels que des apnées ou le syndrome des jambes sans repos.
Les différentes pièces qui constituent le puzzle du sommeil se mettent en place. Aujourd'hui, les recherches sur la fonction du sommeil paradoxal et du rêve reposent sur l'étude, chez l'animal, d'hypersomnies déclenchées par des substances pharmacologiques plutôt que sur les privations de sommeil, dont on ne contrôle pas tous les paramêtres. Ces études nous révèlerons peut-être pourquoi le sommeil paradoxal est apparu si tardivement au cours de l'évolution, avec les oiseaux et les mammifères.
Sommeil calme et sommeil paradoxal
L'enregistrement de l'activité électrique de divers neurones a permis la description des différentes phases du sommeil. Au cours de l'éveil (1), l'activité électrique cérébrale est rapide et de faible amplitude. Le sommeil calme (2) présente des phases de sommeil léger, caracterisé par la présence de "fuseaux" (ou bouffées d'activité de grande amplitude) associés à quelques ondes lentes, et des phases de sommeil profond, ou prédominent les ondes lentes.
Puis survient le sommeil paradoxal (3): il associe des signes du sommeil profond, tel le relachement des muscles (l'electromyogramme est plat) et des signes d'éveil, tels un electro-encephalogramme rapide et des mouvements oculaires. Certains signes sont continus pendant toute la durée du sommeil paradoxal, par exemple l'activité rapide de l'électroencephalogramme et l'atonie musculaire; d'autres sont intermittents, tels les mouvements des yeux, de la face ou des extrémites des membres.
L'activité des neurones nommés SP-ON et SP-OFF est caractéristique du sommeil paradoxal : les neurones SP-ON sont spécifiquement activés au début du sommeil paradoxal et restent actifs pendant toute sa durée, tandis que les neurones SP-OFF s'éteignent progressivement après le début du sommeil paradoxal. Lorsque cesse cette phase du sommeil (4), les neurones SP-ON s'éteignent et les SP-OFF sont réactivés. Les rêves surviennent au cours du sommeil paradoxal. L'activité de certains neurones du corps genouillé lateral, le relais cérébral des voies visuelles est un autre signe du sommeil paradoxal.
1. PHASE D'EVEIL
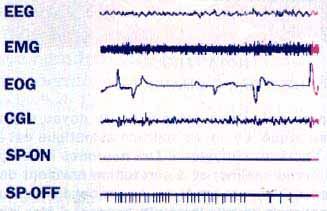
Sur cet enregistrement, la première ligne (l'électroencephalogramme ou EEG) représente l'activité électrique du cerveau (la fréquence des ondes est égale à 20 hertz et leur amplitude a 50*10puissance6 volts environ); EMG (un électromyogramme) indique l'activité des muscles de la nuque; EOG est un électro-oculogramme, indiquant les mouvements des yeux; la quatrième ligne est un enregistrement de l'activité des neurones du corps génouille lateral (CGL), dans le thalamus; la ligne suivante indique l'activité de neurones nommés SP-ON (silencieux pendant l'éveil) et la dernière celle de neurones SP-OFF.
2. PHASE DE SOMMEIL CALME
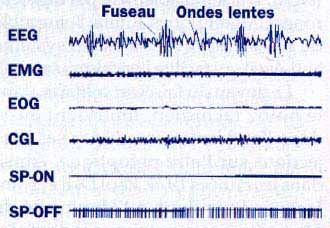
Au cours du sommeil calme, le tonus musculaire faiblit (l'amplitude de l'EMG diminue), les yeux ne bougent pas et les neurones SP-OFF continuent d'être activés. Sur l'électroencephalogramme, on observe des bouffées d'ondes (des fuseaux) séparés par des ondes dites lentes (1 à 4 hertz).
3. PHASE DE SOMMEIL PARADOXAL
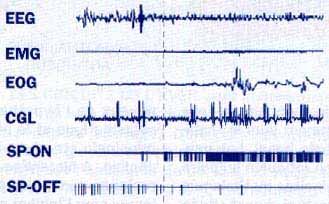
Une phase de sommeil paradoxal suit la phase de sommeil calme (le début est indiqué par la ligne pointillée). L'électroencephalogramme indique une activité cérébrale rapide et de faible amplitude. Le tonus musculaire a disparu, à l'exception de quelques brèves secousses (deuxième ligne). Au cours de cette phase, les yeux bougent (troisième ligne) et les neurones du corps genouillé latéral sont activés (quatrième ligne). Une autre caractéristique du sommeil paradoxal est la mise au repos des neurones SP-OFF et l'activation des neurones SP-ON.
4. FIN DU SOMMEIL PARADOXAL
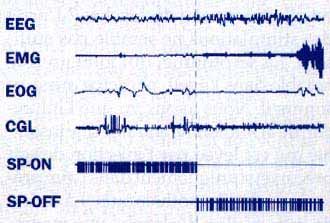
La fin du sommeil paradoxal (à l'endroit de la ligne pointillée) se traduit par une réapparition des fuseaux sur l'électromyogramme, par une diminution de l'activité des yeux, par une mise au repos des neurones SP-ON et par une réactivation des neurones SP-OFF.
A quoi rêvent les chats ?
Au cours du sommeil paradoxal, l'activité électrique venant du cortex moteur est aussi intense que pendant l'éveil actif. mais les motoneurones de la moelle épinière, qui assurent les mouvements, sont silencieux.
Jean-Pierre Sastre de notre laboratoire a décrit le comportement d'animaux qui ont des lesions des neurones responsables de l'inhibition des motoneurones. L'éveil et le sommeil lent ne sont pas modifiés. Le sommeil paradoxal conserve toutes ses caractéristiques, mais le tonus musculaire persiste. Le chat, dont les mouvements ne sont plus inhibés, redresse la tête, se lève, se met a l'affût devant une proie imaginaire, fait le gros dos, le poil hérissé, souffle comme s'il était devant un ennemi, fait sa toilette, ou encore joue avec une balle ou une souris invisibles. La durée (cinq à six minutes) de ces périodes oniriques est identique à celle des phases de sommeil paradoxal enregistrées avant la lésion.
L'expression de ces comportements résulte de l'activation de neurones du système limbique. Le sommeil paradoxal aurait pour fonction, au cours du développement, de mettre en place les circuits dont l'expression est caractéristique de l'espèce. Chez l'adulte, il servirait à les maintenir afin de préserver la personnalité ou à les modifier en fonction de l'experience vécue, pour améliorer l'adaptation à l'environnement.

